Redação –
União Química deve ter reunião com a Anvisa nesta quinta; farmacêutica diz que tem condição de produzir cerca de 8 milhões de doses por mês.
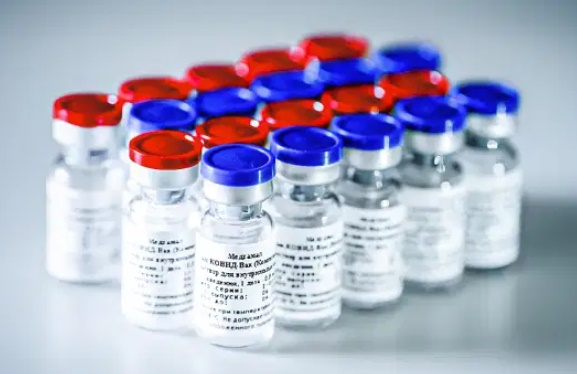
A vacina Sputnik V, que começou a ser distribuída na Argentina em dezembro, poderá ter seu uso emergencial novamente analisado até sexta-feira, dia 22, ou sábado. A expectativa é de uma resposta positiva. Nesta quinta, dia 21, dirigentes da farmacêutica União Química, que deverá fabricar a vacina no Brasil, deverão ter uma reunião com representantes da Anvisa, em Brasília.
Estados como a Bahia e Paraná já fecharam a compra do imunizante. A União Química aguarda apenas o aval da Anvisa para dar início à produção. A empresa informou que tem condições de produzir cerca de 8 milhões de doses por mês.
A Anvisa recusou o pedido de registro do imunizante no último sábado, dia 17, sob a alegação de que não foram testes clínicos no Brasil e faltavam informações sobre o produto. A solcitação de uso emergencial foi protocolada pela União Química em conjunto com o Fundo de Investimentos Diretos da Rússia, que coordenou o desenvolvimento da vacina e é responsável por sua distribuição.
O acerto entre a Bahia e outros estados teria sido diretamente com o fundo, que se comprometeu a providenciar um laboratório no Brasil para fabricar a vacina.
O caso ganhou mais repercusão nesta quarta, quando o ministro Ricardo Lewandowski, do Supremo Tribunal Federaç (STF) determinou que a nova análise sobre o registro da vacina seja feita em até 72 horas, em função de uma ação ajuizada pela Bahia.
O governo do estado pediu ao STF a remoção de restrições à importação de imunizantes contra a covid sem regisro na Anvisa que tenham tido sua utilização autorizada por autoridades sanitárias dos Estados Unidos, União Europeia, Japão, China, Reino Unido ou Irlanda do Norte.
“Considerada a afirmação do autor, feita na petição inicial, de que já foi requerida a autorização temporária para uso emergencial da vacina Sputnik V, informe, preliminarmente, a Agência Nacional de Vigilância Sanitária – Anvisa, no prazo de até 72 (setenta e duas) horas, se confirma tal afirmação e, em caso positivo, esclareça qual o estágio em que se encontra a aprovação do referido imunizante, bem assim eventuais pendências a serem cumpridas pelo interessado”, informa um trecho do despacho do STF.
A Anvisa também solicitou informações adicionais sobre a vacina. A União Química e o fundo de investimento da Rússia disseram que os dados já foram providenciados.
Executivos da União Química estiveram na semana passada em Moscou para tratar dos últimos detalhes sobre a produção das vacinas. A ideia é fabricar pelo menos 10 milhões de doses ainda no Brasil no primeiro trimestre.
Fonte: Revista Exame
MAZOLA
Related posts
Editorias
- Cidades
- Colunistas
- Correspondentes
- Cultura
- Destaques
- DIREITOS HUMANOS
- Economia
- Editorial
- ESPECIAL
- Esportes
- Franquias
- Gastronomia
- Geral
- Internacional
- Justiça
- LGBTQIA+
- Memória
- Opinião
- Política
- Prêmio
- Regulamentação de Jogos
- Sindical
- Tribuna da Nutrição
- TRIBUNA DA REVOLUÇÃO AGRÁRIA
- TRIBUNA DA SAÚDE
- TRIBUNA DAS COMUNIDADES
- TRIBUNA DO MEIO AMBIENTE
- TRIBUNA DO POVO
- TRIBUNA DOS ANIMAIS
- TRIBUNA DOS ESPORTES
- TRIBUNA DOS JUÍZES DEMOCRATAS
- Tribuna na TV
- Turismo